2.14 Výpočet hmotnostní koncentrace roztoku ze zadané hmotnosti rozpuštěné látky a objemu roztoku
Jaká je hmotnostní koncentrace v g⋅l-1 roztoku dusičnanu sodného, jestliže ve 200 ml roztoku je obsaženo 10 g této látky.
Řešení:
 = 200 ml
= 200 ml
m(NaNO3) = 10 g
cm(NaNO3) = g⋅l-1
1. postup – úvahou s využitím přímé úměrnosti
víme, že hmotnostní koncentrace podle (99) udává počet gramů čisté látky (NaNO3) rozpuštěné v 1 dm3
 hledanou hmotnostní koncentraci NaNO3 ve 200 ml = 0,2 l roztoku můžeme vypočítat užitím přímé úměrnosti:
hledanou hmotnostní koncentraci NaNO3 ve 200 ml = 0,2 l roztoku můžeme vypočítat užitím přímé úměrnosti:
10 g .................. 0,2 l 
x g .................. 1 l x : 10 = 1 : 0,2 x = 
x = 50 g NaNO3  cm(NaNO3) = 50 g⋅l-1
cm(NaNO3) = 50 g⋅l-12. postup – dosazením do definičního vztahu
hmotnostní koncentrace je definovaná jako
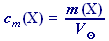 (96)
(96)do vztahu z a. dosadíme zadané hodnoty m(NaNO3) ≐ 10 g a
 = 200 ml = 0,2 l:
= 200 ml = 0,2 l:cm(NaNO3) =
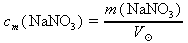 = 50 g⋅l-1
= 50 g⋅l-1
Odpověď: Hmotnostní koncentrace roztoku NaNO3 je 50 g⋅l-1.
2.15 Přepočet hmotnostní koncentrace na molární
Jaká je hmotnostní koncentrace 2,03M roztoku kyseliny dusičné?
Řešení:
c(HNO3) = 2,03 mol⋅dm-3
 = 1,0661 g⋅cm-3
= 1,0661 g⋅cm-3
cm(HNO3) = ?
1. postup – logickou úvahou s využitím dosazení do odvozeného vztahu
víme, že molární koncentrace podle (95) udává počet molů čisté látky (HNO3) rozpuštěné v 1 dm3 roztoku
 1 dm3...........2,03 mol
1 dm3...........2,03 moldále víme, že hmotnostní koncentrace podle (99) udává počet gramů čisté látky (HNO3) rozpuštěné v 1 dm3 roztoku
 hledanou hmotnostní koncentraci zjistíme tak, že látkové množství 2,03 mol obsažené v 1 dm3 roztoku převedeme na hmotnost
hledanou hmotnostní koncentraci zjistíme tak, že látkové množství 2,03 mol obsažené v 1 dm3 roztoku převedeme na hmotnostvyužijeme odvozený vztah (27) pro výpočet hmotnosti m:

do vztahu z c. dosadíme hodnoty n(HNO3) = 2,03 mol z a. a z tabulek M(HNO3) ≐ 63,01 g⋅mol-1:
m(HNO3) = n (HNO3) ⋅ M(HNO3) = 2,03 ⋅ 63,01 ≐ 127,91 g ~ počet gramů čisté HNO3 rozpuštěné v 1 dm3
 c(HNO3) = 127,91 g⋅dm-3
c(HNO3) = 127,91 g⋅dm-3
2. postup – dosazením do odvozeného vztahu
k odvození převodního vzorce využijeme následující vztahy:
definiční vztah (92) molární koncentrace c rozpuštěné látky v roztoku:

odvozený vztah (28) pro výpočet látkového množství n dané látky:

definiční vztah hmotnostní koncentrace cm rozpuštěné látky v roztoku:
 (96)
(96)
provedeme odvození postupným dosazováním vztahů z a. a matematickými úpravami:



 , kde
, kdecm ...................... hmotnostní koncentrace [g⋅dm-3] c ...................... molární koncentrace [mol⋅dm-3] M ...................... molární hmotnost [g⋅mol-1]. do odvozeného vztahu z b. dosadíme zadané hodnoty c(HNO3) = 2,03 mol⋅dm-3 z tabulek M(HNO3) ≐ 63,01 g⋅mol-1:
cm(HNO3) = c(HNO3) ⋅ M(HNO3) = 2,03 ⋅ 63,01 ≐ 127,91 g⋅dm-3
Odpověď: Hmotnostní koncentrace 2,03M roztoku kyseliny dusičné je 127,91 g⋅dm-3.
Servisního střediska pro e-learning na MU.
Technicky realizovala a odpovědnost za funkčnost nese
Veronika Švandová (2008).